上海交大章雪晴团队在Nature Communications发表甾体结构化吸入LNP共递送甾药/抗TSLP mRNA协同治疗难治性哮喘的研究成果
重症哮喘是一种复杂且难治的炎症性疾病,其临床管理面临巨大挑战,尤其是部分患者对糖皮质激素(GC)治疗产生耐药性,导致疾病控制不佳、反复急性加重,严重影响患者预后。研究表明,气道上皮损伤可诱导胸腺基质淋巴细胞生成素(TSLP)异常高表达,通过激活p38 MAPK和STAT3信号轴,促进糖皮质激素受体(GR)磷酸化,进而抑制其核转位,最终削弱GC的抗炎效应,构成GC耐药的重要机制之一。尽管抗TSLP单克隆抗体等抗体疗法已进入临床应用,但其脱靶效应导致的系统性药物蓄积风险,以及肺组织局部药物暴露不足,仍限制了其对局部炎症微环境中TSLP信号的持续抑制效能。因此,亟需开发高效靶向的新型治疗策略,以克服重症哮喘中GC耐药的挑战。
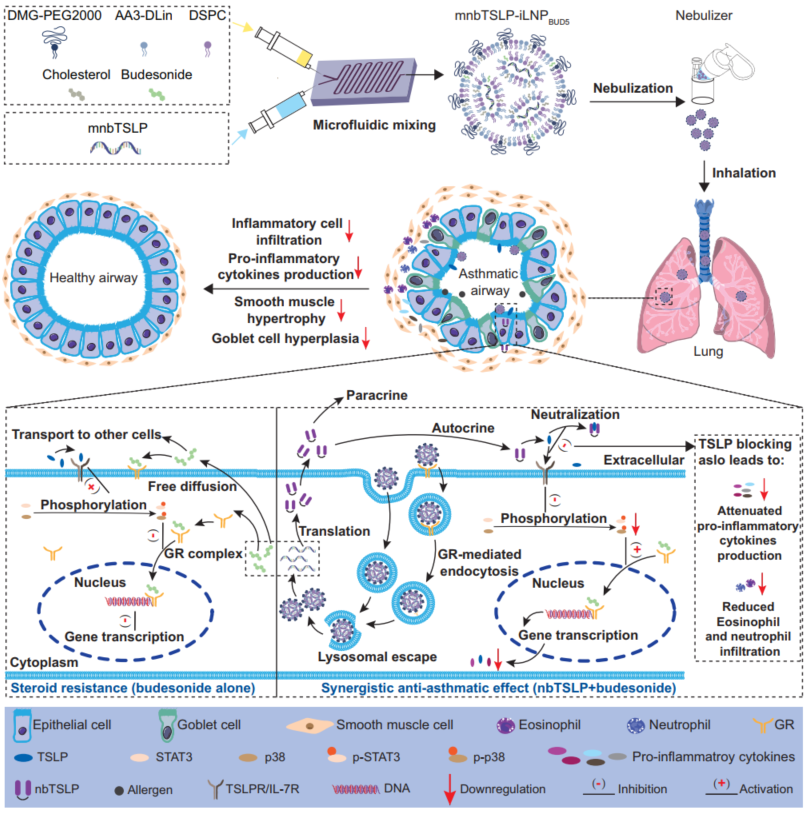
近日,上海交通大学药学院章雪晴教授团队与新泽西理工学院许晓阳教授团队在Nature Communications(《自然·通讯》)上联合发表题为”Budesonide-incorporated inhalable lipid nanoparticles for antiTSLP nanobody mRNA delivery to treat steroid-resistant asthma”的研究论文。该研究创新构建甾体结构化的新型吸入式LNP递送系统(ASCEND),通过布地奈德等甾体分子与脂质骨架的疏水嵌合设计,实现编码抗TSLP纳米抗体mRNA(mnbTSLP)的肺靶向吸入递送。该策略旨在实现甾体抗炎药物与抗体药物在肺部的靶向富集及协同作用,通过调控气道炎症微环境与阻断TSLP介导的2型炎症通路,为重症难治性哮喘提供兼具快速起效与免疫调节优势的创新治疗方案。

在该项目中,研究人员使用布地奈德作为代表性抗哮喘甾体药物,基于其与LNP胆固醇组分的结构相似性,提出以布地奈德部分替代胆固醇作为结构脂质组分,结合制剂优化,成功开发出甾药结构化吸入式LNP(iLNP BUD5)。该iLNP经雾化后粒径、形貌稳定,mRNA包封率无损,且气溶胶可高效介导mnbTSLP在肺部的局部转染、表达和分泌。动物实验结果表明,经雾化给药后,mnbTSLP-iLNP BUD5在肺部呈现显著蓄积,并通过GR介导的内吞途径实现细胞高效摄取和溶酶体逃逸。释放的mnbTSLP在胞质中翻译表达,产生和分泌的nbTSLP纳米抗体可特异性结合并中和细胞外过量的TSLP,阻断其下游信号通路激活;同时,结构整合的布地奈德协同发挥经典的抗炎作用;上述ASCEND策略创新性地将小分子药物与基因治疗相结合,为解决糖皮质激素耐药性重症哮喘提供了新的治疗范式。该递送平台具有以下三个研究亮点:1)通过组分配方、制备工艺、雾化体系等研究变量的多维度协同优化,并在此基础上整合抗哮喘甾体药物为结构成分,构建新型吸入式mRNA-LNP体系,实现小分子和核酸药物针对肺部的精准递送;2)协同抗炎作用:依托载体与核酸药物的协同效应,显著抑制气道炎症及TSLP信号通路,联合疗法显著减轻小鼠模型的气道炎症、重塑和高反应性,且mnbTSLP通过抑制关键炎症通路,恢复哮喘小鼠对布地奈德的敏感性;3)患者依从性高:该策略采用非侵入性吸入给药,操作简便,患者接受度高,具有广阔的临床应用前景。
吸入 mscFv/siPD-L1@LNP 诱导肺部抗肿瘤免疫的示意图
基于新型吸入式肺靶向递送平台ASCEND,载体与所负载的mRNA协同实现难治性哮喘治疗机制突破。研究团队将进一步优化递送系统,推动ASCEND疗法的临床转化,为重症哮喘患者带来更安全、有效的治疗选择。此外,该研究首创的吸入式mRNA-甾体药物联用策略可拓展至慢性阻塞性肺病(COPD)、肺纤维化等呼吸疾病治疗,为呼吸医学临床转化提供了新型递送体系支撑。
原文链接:
https://doi.org/10.1038/s41467-025-61114-4
