上海交大章雪晴团队与新泽西理工学院许晓阳团队在Nature Communications发表mRNA-LNP介导的细胞焦亡疗法以增强肿瘤免疫治疗效果
肿瘤免疫治疗,尤其是免疫检查点阻断(ICB)疗法已成为当前重要的癌症治疗方式,并延长了许多癌症患者的总生存期。然而,只有少数癌症患者(10%-30%的实体瘤患者)对免疫治疗产生完全应答,部分原因是免疫冷肿瘤中存在着高度免疫抑制性的肿瘤微环境(TME)。在肿瘤免疫治疗中,与炎症因子或免疫激动剂协同诱导T细胞免疫应答是缓解免疫抑制、激活T细胞的一种有前景的策略。然而,有效的抗肿瘤免疫需要激活癌症免疫周期的所有步骤,包括免疫原性细胞死亡(ICD)、抗原呈递细胞的成熟、T细胞的启动和活化、肿瘤浸润免疫细胞的募集和炎性细胞因子的产生。但不幸的是,即使是使用多种药物的联合治疗,也常常导致对癌细胞的抑制失败。因此,需要新的治疗策略来诱导有效的抗肿瘤免疫,并拓宽免疫治疗范围。
近日,上海交通大学章雪晴教授、新泽西理工学院许晓阳教授团队合作,在 Nature Communications 期刊发表了题为:mRNA lipid nanoparticle-mediated pyroptosis sensitizes immunologically cold tumors to checkpoint immunotherapy 的研究论文。该研究提出了一种基于mRNA的细胞焦亡纳米药物治疗方法,它能够启动癌症免疫周期,将冷肿瘤转化为炎症细胞因子表达和T细胞浸润的热肿瘤,从而有效治疗免疫冷肿瘤。

细胞焦亡(pyroptosis)是一种炎症性程序性细胞死亡,由gasdermin(GSDM)家族蛋白的蛋白水解性裂解触发。GSDM通常通过其N端和C端结构域的分子内相互作用而自我抑制。在连接区被特异性半胱氨酸天冬氨酸蛋白酶和其他蛋白酶裂解后,坏死性端结构域形成低聚物并转移到质膜。游离N端结构域与脂质成分结合并在细胞膜上并打孔,导致质膜快速破裂,并释放危险相关分子模式(DAMP)和促炎细胞因子。免疫细胞识别特定的DAMP,进而触发一系列免疫反应,包括免疫细胞的激活和浸润。此外,通过焦亡孔释放的促炎细胞因子有助于逆转免疫抑制性肿瘤微环境(TME)。尽管这些发现令人鼓舞,但许多癌症中GSDM的低表达和复杂的裂解过程阻碍了通过递送蛋白酶来触发细胞焦亡以产生抗肿瘤免疫。研究团队推测通过直接传递N末端GSDM结构域诱导的细胞焦亡是在癌症免疫周期中引发一系列事件并将冷肿瘤转化为热肿瘤的有效方法。基于mRNA纳米药物的基因治疗具有广阔的临床应用前景。最近,该成功开发了一种可合成的可电离阳离子脂质纳米颗粒(AA3-Dlin LNPs)的制剂,该制剂具有良好的安全性和较高的体内外mRNA翻译效率。mRNA-LNPs与GSDM协同激活细胞焦亡,有望在肿瘤治疗中发挥重要作用。
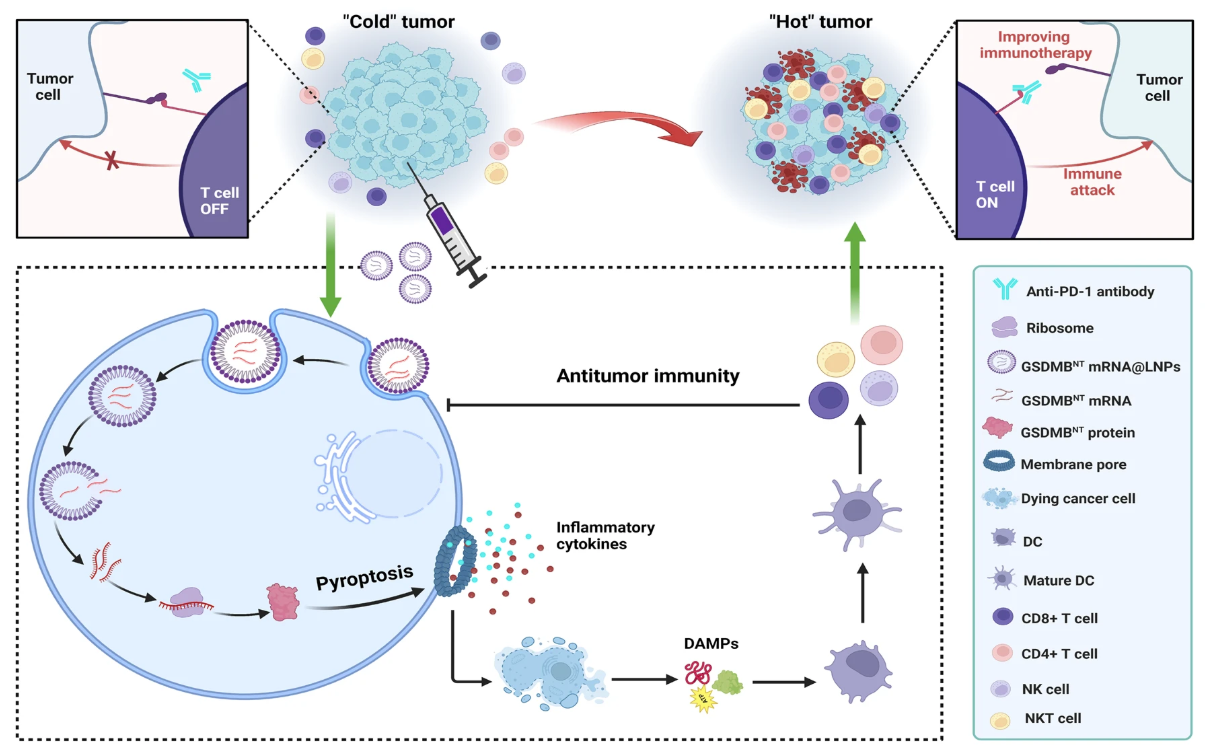
在该研究中,我们提出了一种基于mRNA的纳米医学方法,其中AA3-Dlin LNP配方封装了一个编码GSDMB N-端结构域的单剂mRNA——GSMDBNT mRNA@LNP。开发的GSMDBNT mRNA@LNP配方由可电离阳离子脂质(AA3-Dlin)、磷脂、胆固醇和PEG自组装,GSMDBNT mRNA通过静电相互作用被包裹在LNP内。研究团队期望这种LNP可以被递送到肿瘤组织中,在那里,mRNA被翻译为GSDMB蛋白的端结构域,并直接触发细胞焦亡,而不需要蛋白酶裂解。细胞焦亡具有诱导免疫细胞死亡、启动促炎细胞因子释放以及激活和招募肿瘤内免疫细胞的能力,进而导致一系列事件,进一步促进细胞死亡、细胞因子释放和免疫应答激活。由此产生的正反馈回路可创建有利的免疫原性热肿瘤微环境,使癌细胞对免疫检查点阻断(ICB)介导的免疫治疗敏感,显示出优于单药治疗的肿瘤抑制作用。
论文链接:
https://www.nature.com/articles/s41467-023-39938-9
